Freude bei Bionorica über Cannabis-Entscheidung
21.1.2017, 15:00 Uhr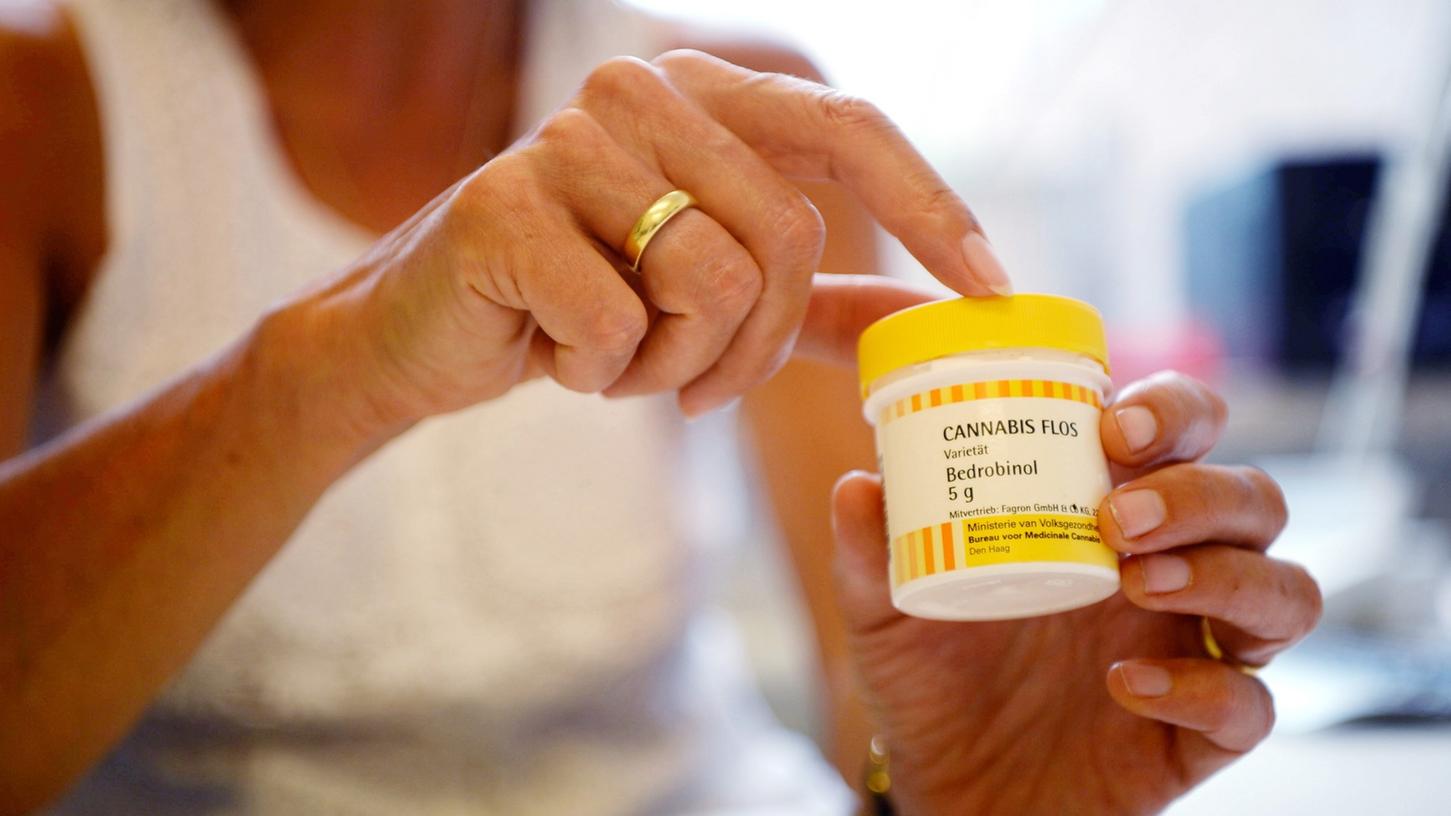
"Dies ist eine historische Entscheidung. Schwerstkranke können voraussichtlich schon ab Februar/ März Cannabis-Arzneimittel auf Rezept erhalten", heißt es vom Neumarkter Unternehmen. Es stellt schon länger solche Medizinprodukte her: "Seit 2002 isoliert Bionorica Dronabinol (THC) aus den Blütenständen von Cannabis-Pflanzen." Als Ausgangsstoff diene Medizinalhanf aus Österreich.
Der Wirkstoff Dronabinol werde zur Linderung von Symptomen bei Schwerstkranken eingesetzt, wie zum Beispiel bei Übelkeit und Erbrechen aufgrund einer Krebs-Chemotherapie, Appetitlosigkeit oder starken chronische Schmerzen.
Nachfrage könnte sich jetzt deutlich erhöhen
Bislang werden die Kosten für den Wirkstoff nur in geschätzt 30 bis 40 Prozent der Fälle von den gesetzlichen Krankenversicherungen erstattet, berichtete Michael Popp, Vorstandsvorsitzender der Bionorica SE im Juli 2016 den NN. Die Nachfrage könnte sich nun nach Verabschiedung der Gesetzesnovelle deutlich erhöhen.
Deshalb wird die Bionorica SE nicht nur seine Produktionskapazitäten anpassen, sondern sie kündigt in ihrer Pressemitteilung auch an "Ärzten und Apothekern, die bisher noch keine Erfahrung mit Dronabinol haben, die nötigen Informationen über den Wirkstoff und sein therapeutisches Potenzial zur Verfügung zu stellen".
Bionorica hat Zulassung beantrag
Denn das Neumarkter Unternehmen liefert bei Vorliegen eines ärztlichen Betäubungsmittel-Rezepts die Reinsubstanz an Apotheken in Deutschland, Österreich und der Schweiz. Diese stellen daraus beispielsweise Tropfen oder Kapseln für ihre Patienten her.
Die Zulassung für ein eigenes fertiges Medikament hat Bionorica bereits 2015 beantragt: Doch bislang wurde es noch nichts mit der Markteinführung von Kachexol – einem Dronabinol-haltigen Fertigarzneimittel, das Übelkeit und Erbrechen im Rahmen einer Krebs-Chemotherapie verringern soll.
Das für die Zulassung zuständige Bundesamt für Arzneimittel und Medizinprodukte hatte den Zulassungsantrag aus formalen Gründen abgelehnt. Seitens des Unternehmens heißt es dazu auf NN-Nachfrage: "Aus unserer Sicht ist die Ablehnung juristisch zweifelhaft, sodass vor dem Verwaltungsgericht Köln ein Klageverfahren eingeleitet wurde, um die Rechtsauffassung der Bundesoberbehörde zu überprüfen".
1 Kommentar
Um selbst einen Kommentar abgeben zu können, müssen Sie sich einloggen oder sich zuvor registrieren.
0/1000 Zeichen



